|
汤文军研究员,博导,课题组长
邮箱: tangwenjun@sioc.ac.cn
办公室电话: 021-54925515
地址:中科院上海有机化学研究所1号楼202
通讯地址: 上海市零陵路345号 200032
|
汤文军博士1974年10月出生于浙江余姚;1995年毕业于华东理工大学精细化工系;1998年于中国科学院上海有机化学研究所获硕士学位;2003年于美国宾夕法尼亚州立大学获博士学位;2003-2005 年在美国Scripps 研究所从事博士后研究;2005-2009年在美国Boehringer Ingelheim药业公司药物工艺部门(Chemical Development) 任高级科学家(Senior Scientist), 在2009-2011年间任首席科学家 (Principal Scientist);2011年7月起任中科院上海有机化学研究所研究员、课题组长;同时兼任上海科技大学物质学院教授、博导、杭州高等研究院首席教授及华东理工大学药学院博导,2015年获中国均相催化青年奖,2017年获国家杰出青年基金资助。2018年入选科技部中青年科技创新领军人才。2019年获药明康德生命化学研究奖学者奖。2024年获得英国皇家化学会学术奖励(RSC Organic Chemistry Horizon Prize)。2025年获得上海市自然科学奖一等奖。 |
1. 发展高效、实用、绿色的催化反应方法学
过渡金属催化是当代有机合成化学中最活跃的领域之一。在过渡金属参与的催化反应中,过渡金属催化剂是整个反应过程的关键,而配体的特性包括电子效应,立体效应,和空间效应直接影响了催化剂的活性和选择性。手性膦配体的发展极大地推动了整个不对称催化领域。在过去的几年中,我们研究小组设计和发展了一系列有显著结构特征的P-手性膦配体在大位阻偶联、不对称偶联、不对称环化、以及不对称氢化中表现出优异的效率,为复杂天然产物和药物的高效合成提供了实用、绿色的催化反应方法学。
|
| 利用我们研究小组发展的合成方法学,开展对一些有重要生理活性天然产物的高效全合成或骨架合成,并进行相关药化研究。以下是我们研究小组已完成的一些天然产物。 |
| 发展能工业化的、高效、经济的新反应或合成策略,实施对药物分子或农药的新工艺研究,非常愿意与有诚意的企业共同研发药物的绿色合成工艺。课题组诚招博士后,有意向者请联系汤文军研究员。 |
 汤文军课题组合影 (2025.12)
汤文军课题组合影 (2025.12)
|
课题组代表性成果:
30. 氢甲酰化反应是一种具有完美原子经济性的,以烯烃和合成气为原料一步合成增加一个碳原子的醛的反应。不对称氢甲酰化反应是从易得原料合成具有高附加值手性分子的最佳方法之一。然而不对称氢甲酰化反应的反应性、区域选择性和对映选择性仍然对底物的空间位阻和官能团高度敏感,并且只有少数手性合成子可以通过不对称氢甲酰化反应有效获得。开发高效、选择性策略以及探索具有新官能团的底物仍然是不对称氢甲酰化反应领域的一个重要目标,带有硼酸酯官能团的底物在不对称氢甲酰化反应中尚未见报道。本课题组、薛小松课题组以及浙江工业大学胡信全课题组合作在烯基硼酸酯的不对称氢甲酰化反应研究中取得进展。本工作首次实现了铑催化烯基硼酸酯的不对称还原氢甲酰化反应。通过采用"伪装"或"直接"还原不对称氢甲酰化策略,开发了以1,2-二硼酸酯取代烯烃或α-硼酸酯取代烯烃为起始原料,铑/(S,S)-Ph-BPE为催化剂,高产率、高对映选择性地对映发散性合成手性γ-硼基醇的方法。该方法有望在学术界和工业界提供一定的合成潜力。该工作发表在《德国应用化学》
Yu, Y.; Zhang, Y.; Xue, X.-S.; Hu, X.; Tang, W.* "Enantiodivergent Rh-Catalyzed Reductive Hydroformylation of Alkenyl Boronic Esters".
Angew. Chem. Int. Ed. 2025, Early View e20602.
[doi]
29. 手性顺式2, 3-二取代哌啶是一类重要的含氮杂环化合物。Sci-Finder搜索显示至今超过 6000 种已知天然产物及超过 300,000 种药物活性分子/中间体具有该手性单元 。如何高效构筑手性顺式2, 3-二取代哌啶结构,高非对称选择性和对映选择性地构筑两个连续手性中心仍然是挑战性课题。发展一个高立体选择性又实用的手性顺式2,3-二取代哌啶化合物的合成方法将同时有助于药物工艺开发和活性小分子的创制。尽管已有较多的非环状不对称反应研究,但是目前为止仅有一例应用于环状含氮化合物的合成,而且未有基于铜催化不对称环化硼胺化反应构筑手性含氮杂环的研究报道。本课题组联合周庆海课题组发展了高效的铜催化不对称环化硼胺化反应,高非对映选择性和对映选择性地构建了一系列手性顺式2, 3-二取代哌啶类化合物。利用易得的含酰氧胺基团的芳基烯烃为原料一步构筑顺式2,3-哌啶结构,通过在硼-铜(I)物种对双键加成过程中引入芳基配位作用,有效控制了反应的区域选择性。以Cu/(S,S)-Ph-BPE为催化体系,具有反应条件温和、官能团耐受性好、区域选择性/非对映选择性/对映选择性优异等特点,实现了抗血管瘤药物ent-Avacopan的关键手性中间体的高效合成。该工作发表在《自然-通讯》上。
Zhang, D.; Yang, H.;* Zhou Q.;* Tang, W.* "Enantioselective synthesis of chiral 2,3-cis-disubstituted piperidines and C1-substituted tetrahydroisoquinolines by asymmetric Cu-catalyzed cyclizative aminoboration".
Nat. Commun. 2025, 16, 6851.
[doi]
28. 含手性季碳中心的α,α-二芳基羰基化合物是一类重要的生物活性分子和药物中间体。手性季碳中心的高效不对称构建是合成化学领域中的一大挑战性研究课题。其中,过渡金属催化的不对称α-芳基化反应是在羰基化合物α-位构建手性季碳中心最直接、高效的合成策略。目前酯的不对称α-芳基化反应仅局限于内酯和活化酯类底物。α,α-二取代非环状酯的不对称α-芳基化反应仍未报道,主要原因是缺乏有效的手性催化剂/配体来解决该类反应的活性和立体选择性问题。本课题组和苏州诺华医药合作首次实现了钯催化的非环状酯类化合物的对映选择性α-芳基化反应,实现了一系列具有手性季碳中心的α,α-二芳基酯类化合物的高效合成。该方法具有底物范围广、条件温和、官能团兼容性强以及低钯负载量(低至 1 mol%)等优点,并成功实现了手性α,α-二芳基γ-丁内酯和局部麻醉药 (R)-amolanone的不对称合成。其中,P-手性单磷配体(R)-3-Pent-BIDIME的发展是该合成方法成功的关键。DFT计算解析了该反应的催化路径并揭示了非共价相互作用在对映选择性控制中的关键作用。该研究拓展了钯催化不对称α-芳基化反应的适用范围,为含手性季碳中心的α, α-二芳基羰基化合物提供了高效的合成方法。该工作发表在《德国应用化学》。
Huang, J. (1st co-author); Pei, C. (1st co-author); Yang, H.;* Wu, B.;* Tang, W.* "Enantioselective Palladium-Catalyzed α-Arylation of Acyclic Esters".
Angew. Chem. Int. Ed. 2025, 64, e202505458.
[doi]
27. 氢甲酰化反应以烯烃、氢气和一氧化碳为原料在过渡金属催化下以完美的原子经济性转化为醛,在有机合成和精细化工领域具有广泛的应用。通过探索金属铑/手性膦配体催化体系发展高效的不对称氢甲酰化反应,实现手性药物或精细化学品的快速合成近年来备受关注,但进展仍然有限。其中四取代烯烃的不对称氢甲酰化反应非常罕见。本课题组和薛小松课题组合作在1,1-二取代烯烃的不对称氢甲酰化反应研究中取得进展。研究采用课题组开发的特色手性双膦配体TFPNH-BIBOP,首次实现了α-取代烯酰胺的铑催化不对称还原氢甲酰化反应,高对映选择性和区域专一性地构建了一系列手性γ-氨基醇,拓宽了不对称氢甲酰化反应的底物适用范围。实验结果和理论计算揭示配体与底物间的氢键相互作用有效促进该催化反应的活性和高对映选择性。该工作原创性膦配体结构的发展以及配体和底物之间相互作用对催化效率的影响为构建更高效的催化体系、进一步拓宽不对称氢甲酰化反应具有指导意义。该工作发表在《美国化学会志》。
Zhu, Y. (1st co-author); Zhang, Y. (1st co-author); He, D.; Yang, H.;* Xue, X.-S.;* Tang, W.* "Rhodium-Catalyzed Asymmetric Reductive Hydroformylation of α-Substituted Enamides".
J. Am. Chem. Soc. 2024, 146, 33249-33257.
[doi]
26. 不对称转移氢化采用甲酸或者醇作为氢源,由于其固有的安全性、操作便利、无需特殊反应装置等特点已经成为合成手性醇和胺不可或缺的重要方法。尤其是Noyori-Ikariya型催化剂在众多不对称转移氢化反应中表现出优秀的对映选择性和宽广的底物适用范围,已经广泛应用于学术研究和工业生产中。然而尽管不对称转移氢化在过去三十多年中取得了较好进展,和不对称氢化的发展相比无论在底物适用范围还是催化剂效率方面仍存在较大差距。适合不对称转移氢化的优秀配体较少,针对不对称转移氢化配体的结构修饰和调控方面的研究不多,可循环使用的负载型Noyori-Ikariya催化剂因效率有限仍未能实现广泛的工业应用。本工作通过双硼介导的不对称还原偶联得到了一系列新型的手性聚合二胺配体,并制备成相应的铱催化剂。该类高效、可循环使用的铱催化剂在众多官能团化酮的不对称转移氢化中表现出优秀的对映选择性(最高可达99% ee)和前所未有的总转化数(12,000转化数,6次循环),展示出良好的工业应用前景。该工作发表在《美国化学会志》。
Lin, Y.; Xu, G.;* Tang, W.* "Chiral Polymeric Diamine Ligands for Iridium-Catalyzed Asymmetric Transfer Hydrogenation".
J. Am. Chem. Soc. 2024, 146, 27736-27744.
[doi]
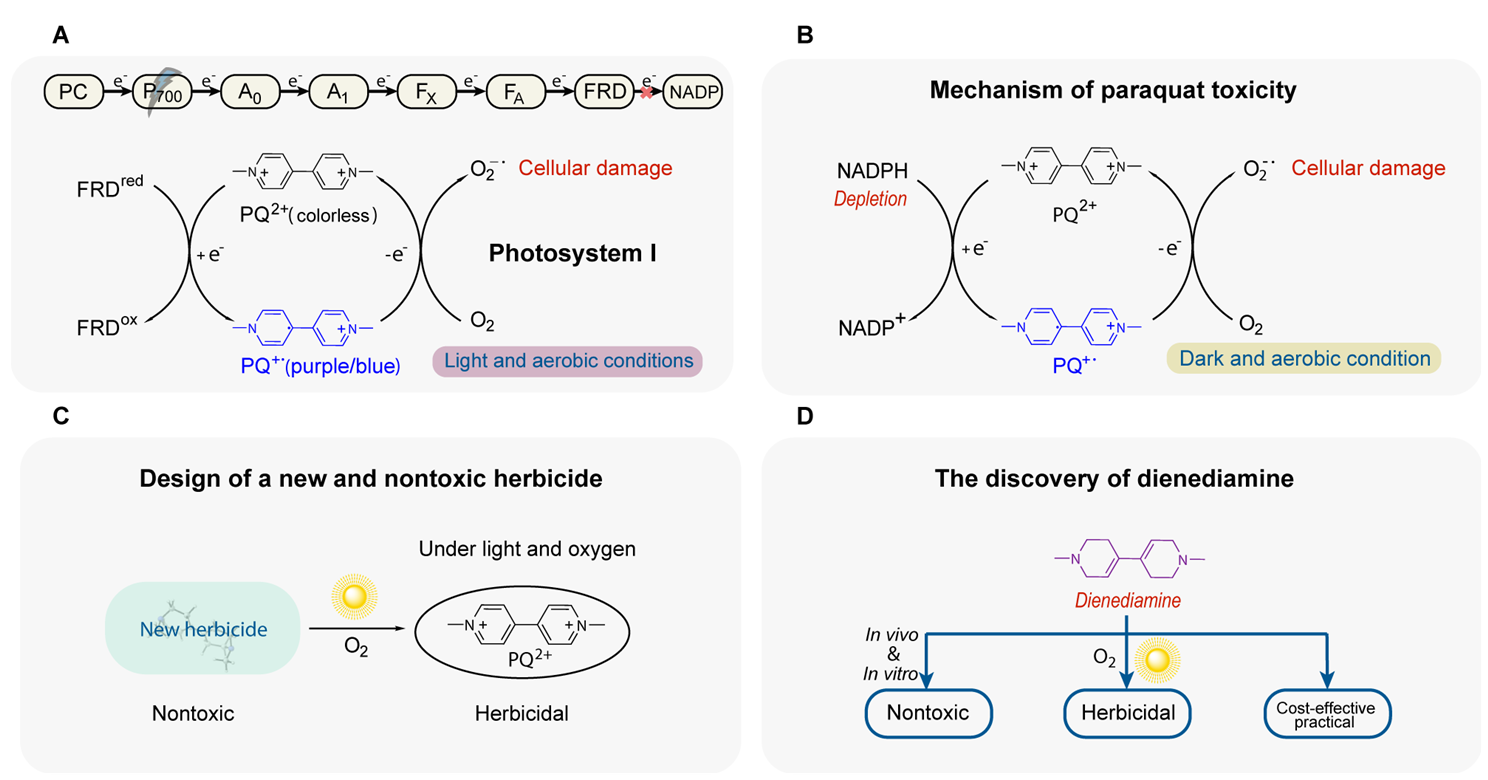
25. 百草枯由于其除草迅速、高效、广谱、成本低廉、对植物根系无毒性等优点,自1962年上市以来迅速成为广泛应用于全球的除草剂。然而百草枯的另一个名字为“杀人农药”。这不仅是因为百草枯对动物和人有剧毒,大鼠口服LD50剂量为100 mg/kg,而且因为没有有效的解毒剂,中毒死亡率为50~90%。迄今,全球至少数万人因自杀或误食百草枯而死亡。因此发展一种和百草枯除草效果相比拟的安全除草剂,是学术界和工业界共同追求的目标。 本课题组与同济大学附属第十人民医院彭艾教授团队合作创制了新型除草剂双烯双胺。研究发现,双烯双胺表现出和百草枯相当的除草效果,并通过一系列小鼠和细胞实验表明较好的安全性,有望成为一种替代百草枯、安全无毒的新型绿色除草剂。该工作发表在植物科学领域顶级期刊《分子植物(Molecular Plant)》上。
Peng, H.(1st co-author); Zhao, D.(1st co-author); Tang, W.*; Peng, A* “Dienediamine: A Safe Herbicide as Paraquat Surrogate”.
Mol. Plant. 2023, 16, 1962-1975. [doi]
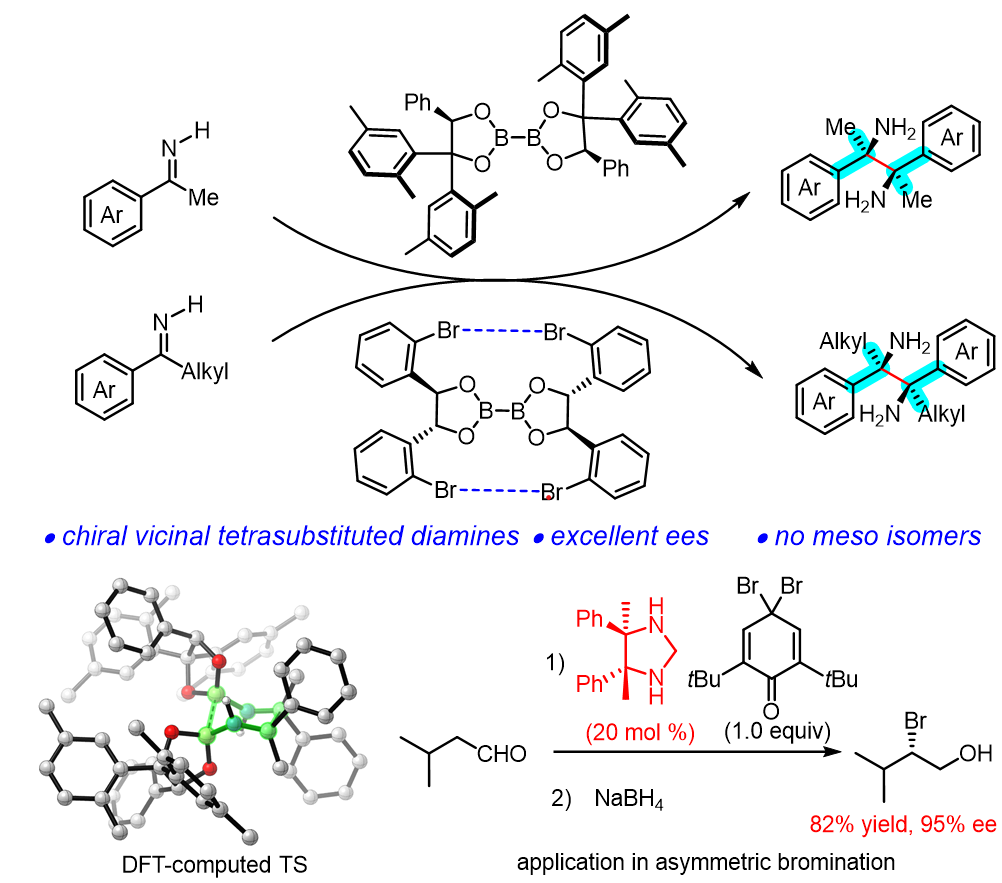
24. 手性邻二胺近年来逐渐成为药物、生物活性分子、功能材料和金属有机催化剂的重要合成砌块,也更多地用作手性的有机小分子催化剂。在过去数十年里化学家们发展了许多合成手性邻二胺的方法包括一系列高效的不对称催化反应。然而,绝大多数已知的方法局限于邻位单或双取代的手性邻二胺的合成,对于邻位四取代邻二胺的不对称合成鲜有报道。近日本课题组与南方科技大学化学系钟龙华教授合作,报道了新型手性双硼介导芳基烷基酮亚胺的不对称还原偶联,合成了一系列前所未有的手性大位阻邻位四取代邻二胺,反应中无内消旋化合物产生。该方法具有实用、广谱、简单、高效等特点,表现出优异的非对映选择性和对映选择性。该工作发表在《德国应用化学》。
Zhou, M.(1st co-author); Lin, Y.(1st co-author); Chen, X.-X.(1st co-author); Xu, G.;* Chung, L. W.;* Tang, W.* "Asymmetric Synthesis of Vicinal Tetrasubstituted Diamines via Reductive Coupling of Ketimines Templated by Chiral Diborons".
Angew. Chem., Int. Ed. 2023, 62, e202300334. [doi]
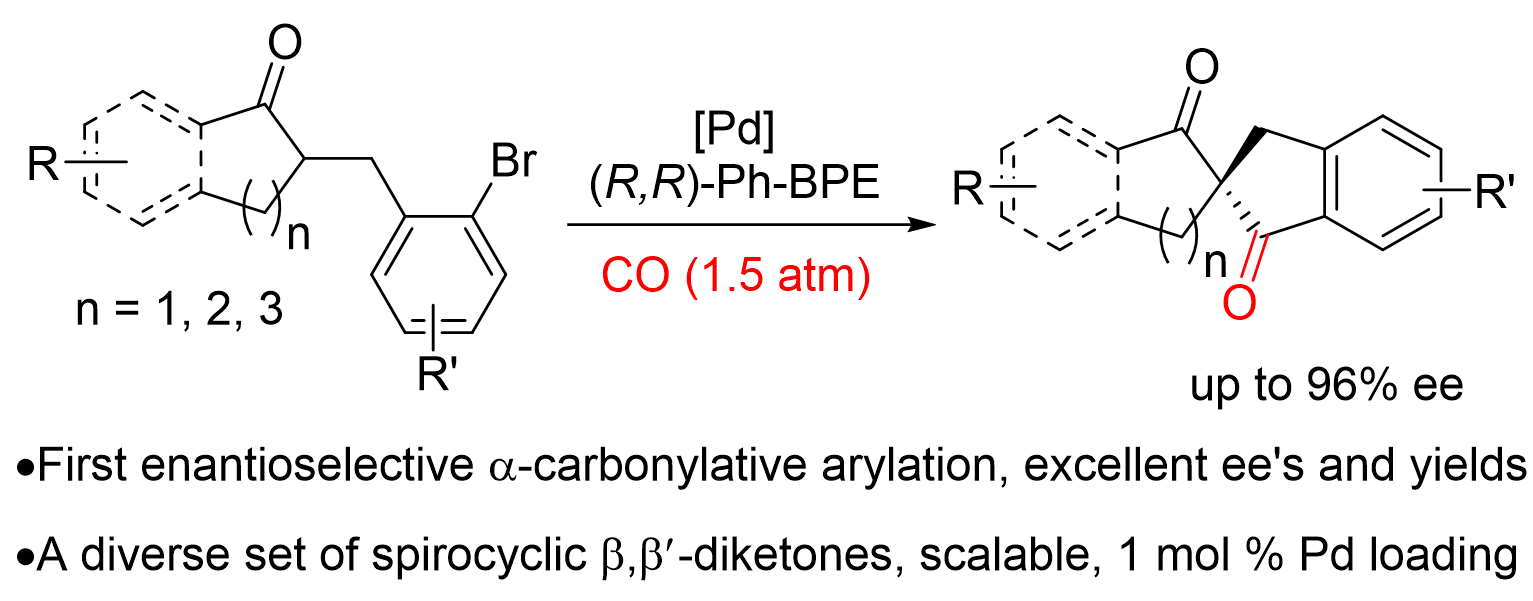
23. α-插羰芳基化反应既是常见的α-芳基化反应范畴的延伸,又是羰基化反应类型的扩展,是构建丰富多彩的1,3-二酮类结构的有效方法。目前,该反应多受限于分子间反应,且仅用于消旋产物的合成。手性β,β’-螺环二酮单元是重要的配体前体,其中羰基是活性反应官能团,可用于后续转化制备多个有应用价值的结构单元。时至今日,仍然缺乏对该类结构有效的催化不对称合成方法。本工作实现了首例过渡金属催化的不对称α-插羰芳基化反应,采用钯催化剂和膦杂环戊烷类双膦配体(R,R)-Ph-BPE,在4Å分子筛的促进下,以中等到优秀的收率和对映选择性实现了一系列C1和C2对称的螺环二酮骨架的高效合成,该反应具有较好的底物普适性和官能团耐受性。该工作发表在《德国应用化学》。
Wu, T.; Zhou, Q.; Tang, W.* "Enantioselective α‐Carbonylative Arylation for Facile Construction of Chiral Spirocyclic β,β'‐Diketones".
Angew. Chem., Int. Ed. 2021, 60, 9978-9983. [doi]
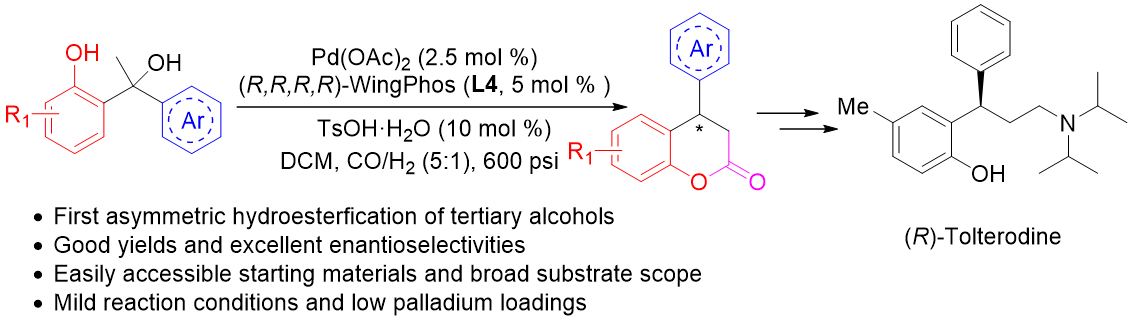
22. 烯烃的氢酯化反应(Reppe反应)是过渡金属催化下将烯烃、一氧化碳和醇转化为具有高附加值的羰基化合物的重要手段,已经广泛应用于药物、材料及精细化学品的工业生产中。然而,由于缺乏高效高立体选择性的催化体系,不对称氢酯化反应依然发展缓慢,特别是三级醇的不对称氢酯化反应至今未有报道。本课题组利用所发展的(R,R,R,R)-WingPhos配体首次实现了二芳基烷基甲醇的钯催化不对称氢酯化反应。利用该方法,一系列手性4-芳基-3,4-二氢香豆素类化合物可以在温和的反应条件和低催化剂当量下以优秀的收率和对映选择性顺利获得。另外,利用该反应从简单二芳基烷基甲醇化合物出发可以实现GPR40 激动剂和药物分子(R)-Tolterodine的高效合成。该反应的实现不仅为手性4-芳基-3,4-二氢香豆素类化合物的合成提供了一种简便的方法,而且进一步填补了不对称氢酯化反应的空白。该工作发表在《德国应用化学》。
Tian, D,; Xu, R,; Zhu, J.; Huang, J.; Dong, W.; Claverie, J.; Tang, W.* "Asymmetric Hydroesterification of Diarylmethyl Carbinols".
Angew. Chem., Int. Ed. 2021, 60, 6305-6309. [doi]
21. 手性1,2-二胺结构广泛存在于天然产物、医药和农药分子中,含有手性1,2-二胺结构的配体和金属络合物在不对称催化领域中发挥着不可替代的作用。研究团队在这份工作中设计并合成了大位阻的手性联硼酸酯试剂,可以与双亚胺分子配位,经六元环椅式构象过渡态,实现高立体选择性的还原偶联。该方法学具有对映选择性和立体专一性高、反应条件温和、操作步骤简单、使用现成的起始材料、底物适用范围广等特点。此项工作将大幅度促进手性1,2-双胺相关的化学研究,并进一步巩固了联硼参与的周环反应的实验和理论基础。该工作发表在《美国化学会志》。
Zhou, M.; Li, K.; Chen, D.; Xu, R.; Xu, G.* Tang, W.* "Enantioselective Reductive Coupling of Imines Templated by Chiral Diboron".
J. Am. Chem. Soc. 2020, 142, 10337-10342. [doi]
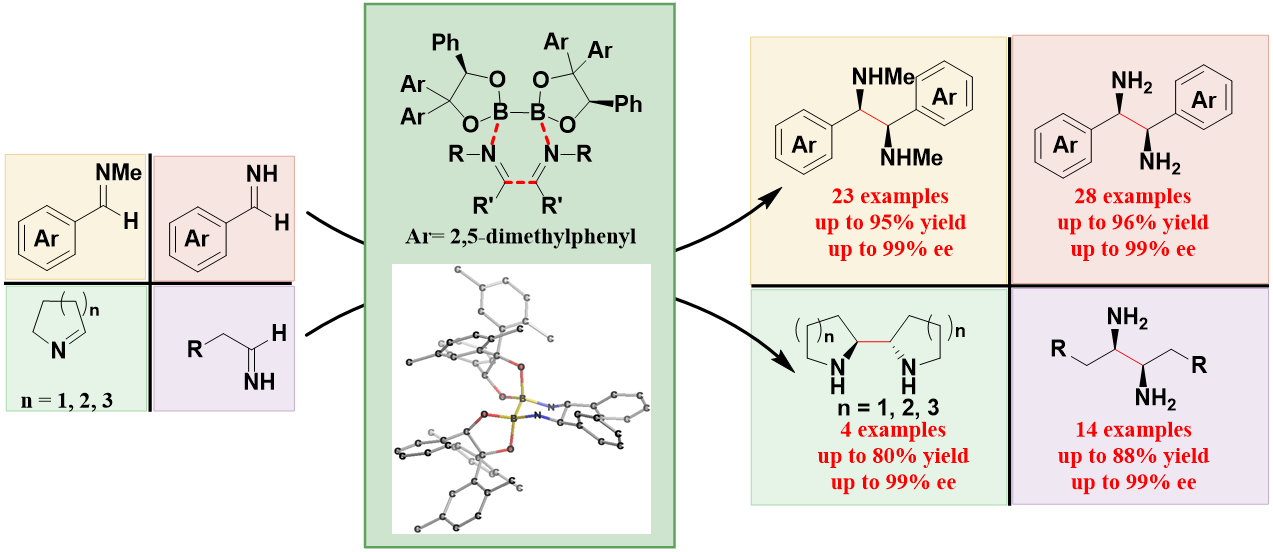
20. 具有轴手性的联芳基结构广泛存在于药物和天然产物分子中。许多具有独特优势的手性催化剂和配体也是基于轴手性的联芳基骨架发展而来。在所有构建轴手性联芳基结构的策略中,不对称偶联无疑是最为简洁且直接的方法。通过不对称偶联合成具有轴手性的联芳基结构,尤其是含有邻位四取代联芳基化合物的挑战在于提高偶联反应的反应活性和对映选择性的高效调控。本工作通过发展新型手性配体和设计新的反应模式,成功发展了用于高效合成邻位四取代联芳基结构的不对称Suzuki-Miyaura偶联反应。基于此方法,我们合成了一系列邻位四取代联苯基和联萘基的独特结构。同时我们也实现了棉酚的高效不对称全合成。该工作发表在《美国化学会志》。
Yang, H.; Sun, J.; Gu, W.; Tang, W.* "Enantioselective Cross-Coupling for Axially Chiral Tetra-ortho-Substituted Biaryls and Asymmetric Synthesis of Gossypol".
J. Am. Chem. Soc. 2020, 142, 8036–8043. [doi]
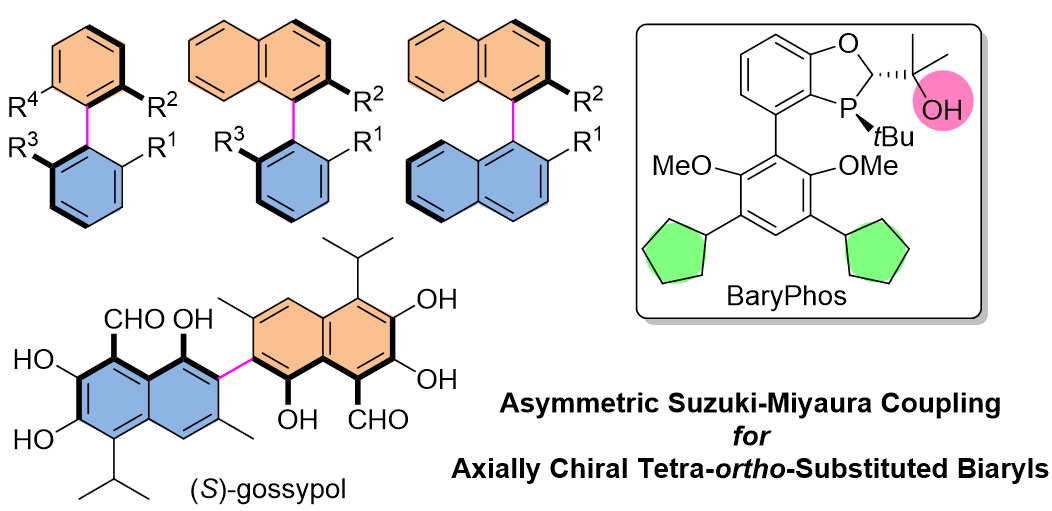
19. 许多具有重要生物活性的复杂天然产物都含有芳基季碳中心的桥联多环骨架,如止痛药吗啡(morphine)、石蒜科生物碱中文殊兰碱(crinine)、抗丙型肝炎二萜烯十一醇(elevenol)、高异黄烷10,11-dihydroxydracaenon C、吲哚二萜类tubingensin B和吲哚生物碱aspernomine。尽管在复杂多环天然产物的合成方面已取得了巨大的进步,但仍然缺乏有效且通用的方法来合成含有全碳四元中心桥联多环骨架。在此,我们课题组报道了一种简便而通用的方法,通过钯催化的去芳化环化反应构建多种桥联多环骨架的衍生物。该工作发表于《德国应用化学》。
Mu, X.; Yu, H.; Peng, H.; Xiong, W.; Wu, T.; Tang, W.* "Expedite Construction of Various Bridged Polycyclic Skeletons by Palladium-Catalyzed Dearomatization".
Angew. Chem., Int. Ed. 2020, 59, 8143-8147. [doi]
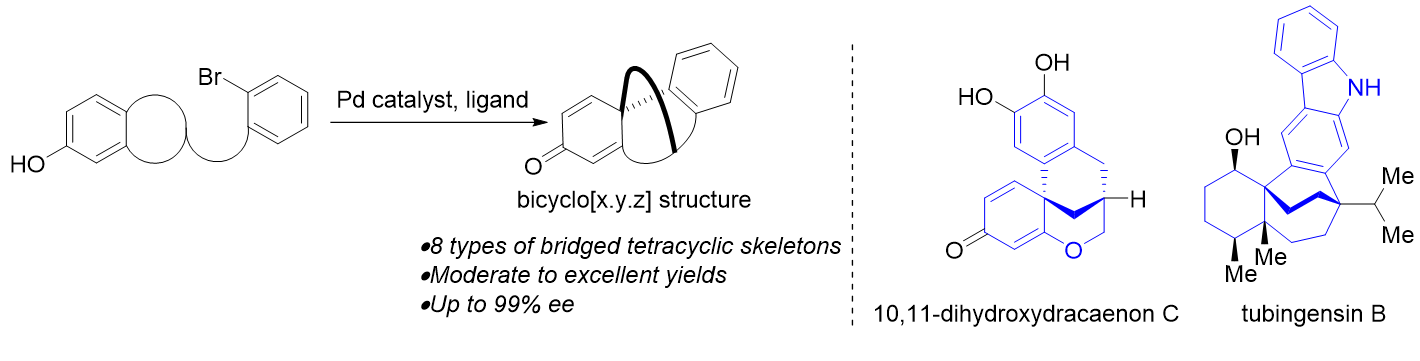
18. 手性α-三级胺是许多具有重要生物活性的天然产物分子和药物分子中都有的结构片段。合成手性α-三级胺的主要方法之一是有机硼试剂对酮亚胺的不对称加成。尽管近些年在芳基硼试剂对芳基酮亚胺的不对称加成方面取得了巨大的进展,但是无一例外,所有的芳基酮亚胺底物均使用保护基保护,由于保护基的脱除需要剧烈的条件,使得产物的进一步转化面临巨大困难,限制了实际应用。我们基于本课题组发展的BIBOP骨架配体具有的明显优势,实现了芳基硼试剂对无保护酮亚胺的高立体选择性的不对称加成,获得了具有潜在药用价值的两类手性α-三级胺产物。这一方法学也成功地应用于高抗疟活性分子Cipargamine的合成。该工作发表在《德国应用化学》。
Zhu, J.; Huang, L.; Dong, W.; Li, N.; Yu, X.; Deng, W.*; Tang,W.* Enantioselective Rhodium-Catalyzed Addition of Arylboroxines to N-Unprotected Ketimines: Efficient Synthesis of Cipargamine
Angew. Chem., Int. Ed. 2019, 58, 16119-16123. (highlighted as Angew. Chem., Int. Ed. VIP Paper) [doi]
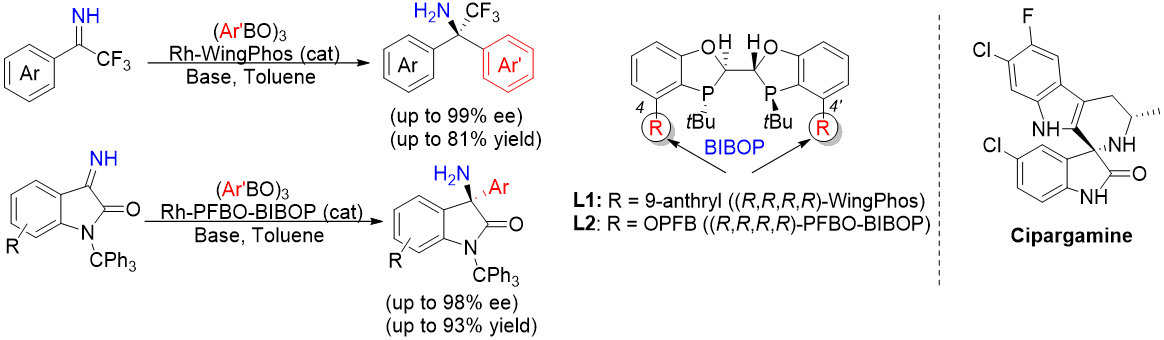
17. 我们在配体设计中创造性地引入了立体电子效应控制因素,设计了大位阻、富电子、C2-对称的P手性双膦配体,ArcPhos。由此,我们得到含有2个磷手性中心,4个碳手性中心的具有深的手性口袋的铑催化剂Rh[ArcPhos(nbd)]SbF6。在四取代碳环或杂环烯酰胺底物的催化不对称氢化反应中,催化剂显示出卓越的对映选择性(ee达到99%)和转化数(TONS达到10000),从而得到一系列cis-2-烷基取代的碳环或杂环胺衍生物。通过机理探究,我们认为反应通过“dihydride”路径进行,酰胺的双键的配位步骤为对映决定步。这一方法学也成功应用于Janus激酶抑制剂Tofacitinib(托法替尼)的合成中。该工作目前被《德国应用化学》接收。
Li, C.(1st co-author); Wan, F.(1st co-author); Chen, Y.; Peng, H.; Tang, W.*; Yu, S.*; McWilliams, J. C.*, Mustakis, J.; Samp, L.; Maguire, R. J. Stereoelectronic Effects in Ligand Design: Enantioselective RhodiumCatalyzed Hydrogenation of Aliphatic Cyclic Tetrasubstituted Enamides and Concise Synthesis of (R)-Tofacitinib
Angew. Chem., Int. Ed. 2019, 58, 13573-13583. [doi]

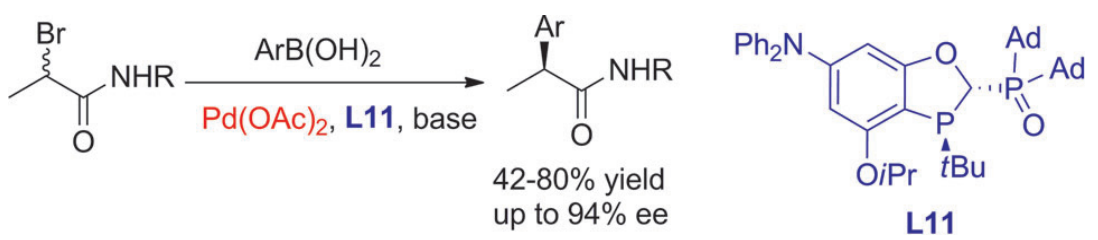
16. 手性α-芳基羰基片段广泛存在于天然产物及药物分子结构中。高效合成手性α-芳基羰基片段一直是有机化学领域中的热点问题。我们提出大位阻P,P=O配体能有效抑制二次转金属:1)大位阻P,P=O配体中氧可以和钯中心有弱配位作用,导致二价钯物种C的位阻增大,提高了二次转金属中过渡态CD的能垒,从而可以有效抑制二次转金属;2)由于氧和钯中心的弱配位作用,大位阻P,P=O配体仍然有足够的活性实现烷基芳基的偶联;3)手性大位阻P,P=O配体能够实现不对称的烷基芳基偶联。我们因此发展了手性大位阻P,P=O配体L11并首次实现了钯催化α-溴代酰胺与芳基硼酸的不对称交叉偶联反应,催化剂当量最低可降至0.5 mol %。以N-CH(2-MeOPh)2作为酰胺取代基,醋酸钯和配体作为催化剂,在氟化钾的作用下能够以良好的收率和优秀的对映选择性得到手性的α-芳基酰胺类化合物。相关工作发表在《德国应用化学》上。
Li, B.; Li, T.; Aliyu, M. A.; Li, Z.; Tang, W.* Enantioselective Palladium-Catalyzed Cross-Coupling of a-Bromo Carboxamides and Aryl Boronic Acids.
Angew. Chem., Int. Ed. 2019, 58, 11355-11359. [doi]
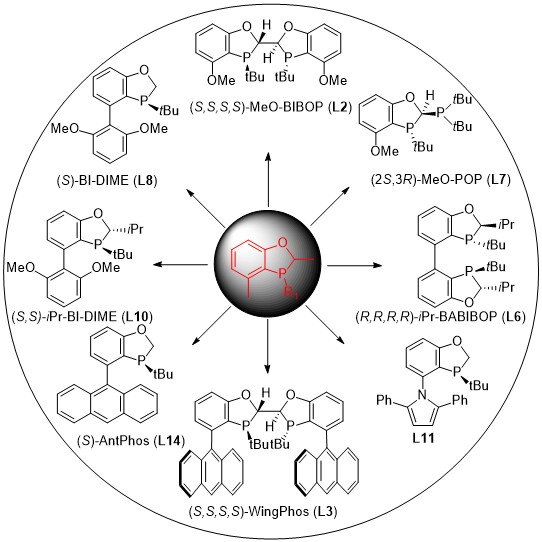
15. 在过渡金属参与的不对称催化反应中,过渡金属催化剂是整个反应过程的关键,而与过渡金属配位的手性配体直接影响了催化剂的活性和选择性。设计和发展结构特征新颖的配体对于发现新反应、提高现有反应的效率和实用性具有十分重要的意义。P-手性膦配体由于手性中心直接和过渡金属配位,所构筑的手性环境最靠近底物和反应中心,理论上最容易表现出优秀的选择性。然而,由于合成上的困难,P-手性膦配体的发展至今缓慢。本课题组在过去几年中致力于发展一类实用又高效的P-手性膦配体。本课题组介绍了如何从一个手性氧杂膦烷结构发展出一系列具有重要学术和应用价值的手性双膦和单膦配体的研究理念。这些膦配体具有构象单一、电性和位阻灵活可调、稳定可操作性强等特征。其中手性双膦配体MeO-BIBOP、WingPhos 和iPr-BABIBOP在不对称氢化和其他反应中表现出优秀的立体选择性和非凡的转化数,能用来合成各类手性中间体,具有重要的工业应用价值。以BI-DIME、AntPhos和iPr-BI-DIME为代表的P-手性联芳基单膦配体功能强大、应用性极广,在众多不对称催化反应中,尤其是高难度的不对称大位阻偶联中,表现出独特的效率和选择性。这些配体已经应用于许多复杂分子全合成和药物工艺研究中,可以预见这些配体在今后的不对称催化和药物工艺研究中将发挥更大的作用、展示更多的功能。
Xu, G., Chris H. Senanayake.; Tang, W.* P-Chiral Phosphorus Ligands Based on a 2,3-Dihydrobenzo[d][1,3]oxaphosphole Motif for Asymmetric Catalysis.
Acc. Chem. Res. 2019, 52, 1101−1112.[doi]
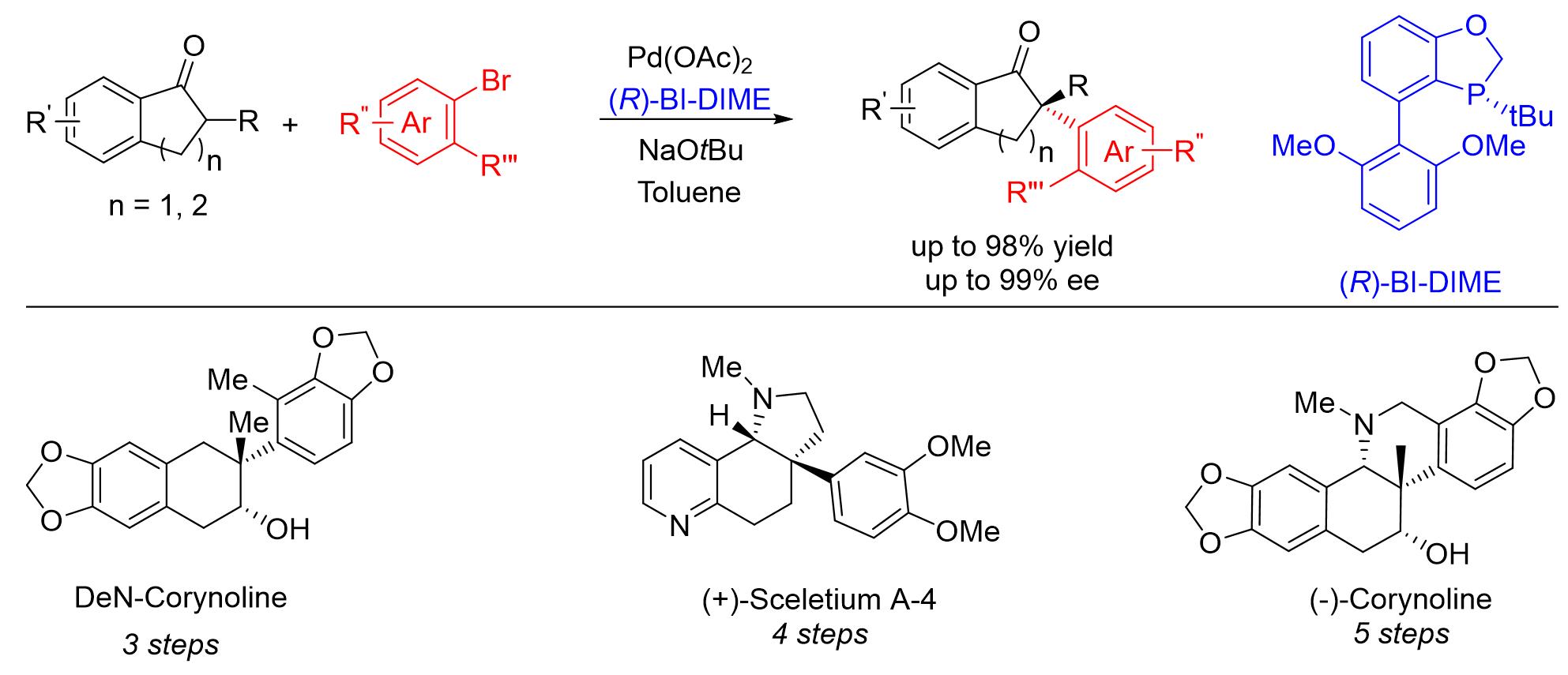
14. 苄位手性季碳中心结构广泛存在于众多天然产物及具有药物活性的分子结构中,然而此类手性骨架的高效合成一直以来是有机化学界中的难题。钯催化不对称α-芳基化反应是合成苄位手性季碳中心结构的较为理想而又简便的方法,但是现有合成方法仍然具有较大的局限性,尤其对具有较大位阻的芳基卤化物反应产率和立体选择性均不理想,限制了不对称α-芳基化反应在天然产物和药物分子合成中的广泛应用。我们小组成功地将手性BI-DIME配体应用于钯催化的大位阻α-芳基化反应中,在温和的反应条件以及较低的催化剂用量下,合成了一系列具有苄位手性季碳中心结构、大位阻的芳香环酮衍生物。并且我们以不对称α-芳基化反应为主要合成策略,从简单易得的原料出发仅5步实现了(-)-紫堇灵的高效不对称合成,并以3步反应制备了同样具有重要生理活性的deN-Corynoline,用4步合成了天然产物(+)-Sceletium A-4。此项工作近期发表在《德国应用化学》。
Rao, X(1st co-author).; Li, N(1st co-author).; Bai, H(1st co-author).; Wang, Z.; Tang, W.* Efficient Synthesis of (-)-Corynoline by Sterically Hindered Enantioselective Palladium-Catalyzed α-Arylation.
Angew. Chem., Int. Ed. 2018, 57, 12328 –12332.[doi]
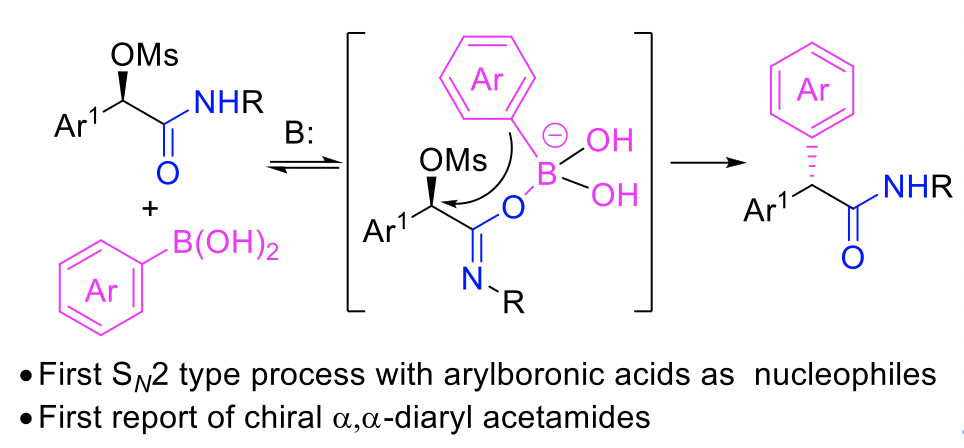
13. 手性的α,α-二芳基酰胺结构广泛存在于天然产物和药物分子中,因此发展高效、实用的立体专一C(sp2)-C(sp3)偶联反应并用于手性α,α-二芳基酰胺结构的构建一直是有机化学领域中的重要研究课题。我们小组发展了一种高效的无金属参与的C(sp2)-C(sp3)偶联反应,首次以芳基硼酸作为亲核试剂对sp3杂化的碳原子进行SN2进攻,以温和的反应条件,较好的官能团兼容性顺利得到二芳基酰胺产物。并且,我们将该方法学应用在大麻素受体配体 CB1-receptor,抗抑郁活性分子(S)-diclofensine和降血脂药 implitapide关键中间体的合成中。此项工作近期发表在《德国应用化学》。
Tian, D(1st co-author).; Li, C(1st co-author).; Gu, G.; Peng, P.; Zhang, X.;* Tang, W.* Stereospecific Nucleophilic Substitution with Arylboronic Acids as Nucleophiles: A Crucial CONH Effect.
Angew. Chem., Int. Ed. 2018. 57, 7176-7180. [doi]
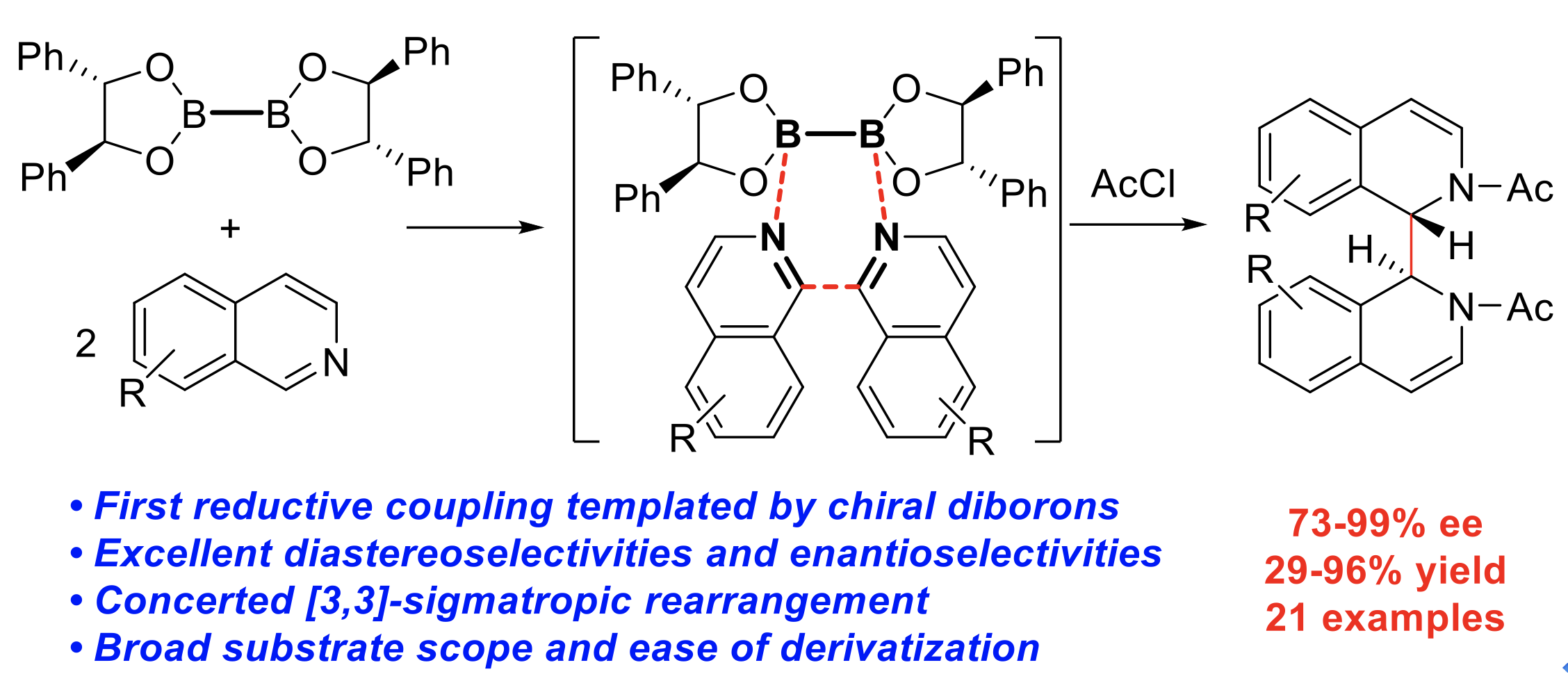
12. 联硼酸酯化合物作为制备芳基或烷基硼酸酯的重要合成原料广泛应用于工业中,然而利用其还原性在无过渡金属参与下实现碳碳键偶联则鲜有报道。利用简便易得的手性联硼酸酯实现高立体选择性的偶联反应将是很有吸引力的化学,而且具有实用价值。我们课题组首次发现联硼酸酯可以在温和条件下促进异喹啉的高效还原偶联,并高产率、高非对映选择性地实现了外消旋双异喹啉的制备;在此基础上,他们利用手性联硼酸酯,进一步实现了一系列手性双异喹啉类化合物的高对映选择性合成,底物适用范围广,官能团容忍性佳;通过一系列机理实验包括电子顺磁共振实验以及计算化学等,首次提出联硼参与的[3,3]- σ重排反应新模式,为进一步拓宽手性联硼酸酯介导的高立体选择性还原偶联反应提供理论基础。此项工作近期发表在美国化学会志上。
Chen, D.; Xu, G.; Zhou, Q.; Chung, L, -W.; Tang, W.* Practical and Asymmetric Reductive Coupling of Isoquinolines Templated by Chiral Diborons.
J. Am. Chem. Soc. 2017, 139, 9767-3363. [doi]
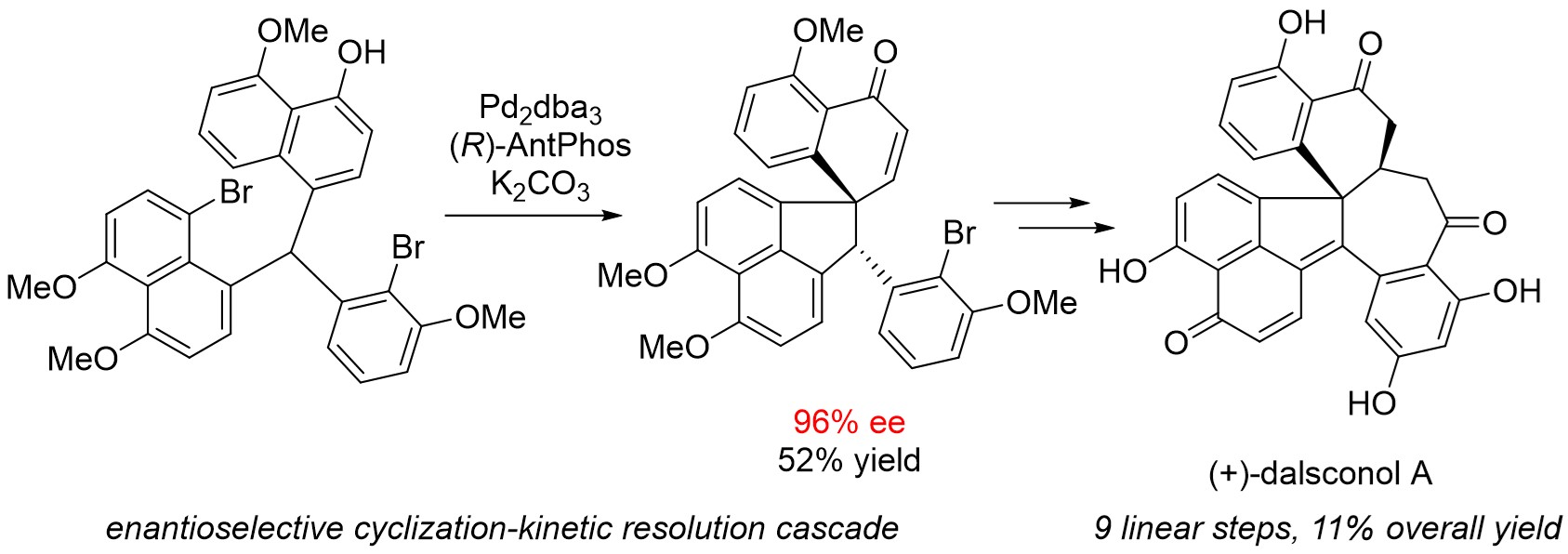
11. Dalesconol A和B是具有强免疫抑制作用的聚酮类天然产物,天然的Dalesconol A和B均为两个对映异构体的非消旋混合物,天然的混合物比光学纯的对映异构体具有更强的抗免疫活性。实现Dalesconol A和B的不对称合成不仅可进一步研究其光学纯化合物的生物活性,同时也可为开发相关类似结构的免疫抑制剂提供有效技术路线支持。我们课题组利用不对称去芳构偶联为主要合成策略仅用九步高效完成了Dalesconol A和B的首次不对称合成,该工作将积极推动新型免疫抑制剂的研究和发展。此项成果近期发表在美国化学会志上。此项工作近期发表在美国化学会志上。
Zhao, G(1st co-author).; Xu, G(1st co-author).; Qian, C.; Tang, W.* Efficient Enantioselective Syntheses of (+)-Dalesconol A and B.
J. Am. Chem. Soc. 2017, 139, 3360-3363.
[doi]
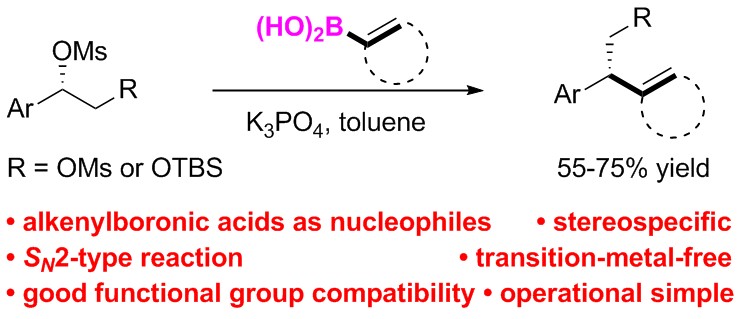
10. 高效的立体专一C(sp2)-C(sp3)偶联反应对于天然产物和药物分子的合成具有重要意义,因此发展高效、实用的立体专一C(sp2)-C(sp3)偶联反应一直是有机化学领域中的重要研究课题。相比于传统的过渡金属催化饱受β氢消除问题困扰,以及传统的锂试剂或者格式试剂参与的SN2反应官能团兼容性较差等问题,我们小组发展了一种高效的无金属参与的C(sp2)-C(sp3)偶联反应,首次以硼酸作为亲核试剂对sp3杂化的碳原子进行SN2进攻,以温和的反应条件,较好的官能团兼容性顺利得到一系列立体专一的手性产物。此项工作近期发表在美国化学会志上。
Li, C.; Zhang, Y.; Sun, Q.; Gu, T.; Peng, H.; Tang, W.* Transition-Metal-Free Stereospecific Cross-Coupling with Alkenylboronic Acids as Nucleophiles.
J. Am. Chem. Soc. 2016, 138, 10774-10777.
[doi]
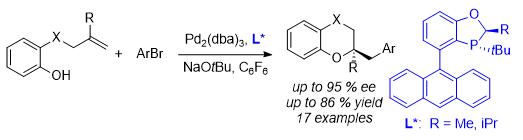
9. 许多具有生物活性的天然产物或药物含有手性的1,4-苯并二氧六环或苯并吡喃单元。因此,不对称合成手性1,4-苯并二氧六环或苯并吡喃单元获得了极大的关注。钯催化的烯烃芳氧基芳基化反应是含有端位烯烃的苯酚和芳基卤化物之间的偶联反应。该反应的优点是能从简单易得的原料直接合成2-取代苯并吡喃单元。然而对映体选择性的烯烃芳氧基芳基化反应至今未能实现,关键的问题还是缺少一个理想的手性催化剂。课题组设计开发了新型的单膦配体首次实现了高立体选择性的烯烃芳氧基芳基化反应,实现了对一系列1,4-苯并二氧六环或苯并吡喃以及苯并异噁嗪的高立体选择性合成。此项工作近期发表在《德国应用化学》。
Hu, N.; Li, K.; Wang, Z.; Tang, W.* Synthesis of Chiral 1,4-Benzodioxanes and Chromans by Enantioselective Palladium-Catalyzed Alkene Aryloxyarylation Reactions.
Angew. Chem., Int. Ed. 2016, 55, 5044–5048. [doi]
 |
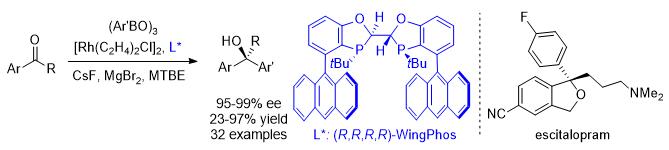
8. 手性二(杂)芳基叔醇是许多重要生物活性分子或药物的结构片段。例如组胺H1受体拮抗剂卡比沙明,抗抑郁药物艾司西酞普兰和生长激素SM-130686都具有这类手性三级醇的关键结构。一个最理想、经济和环境友好的合成方法是芳基硼试剂对简单酮的不对称加成。然而,这个加成反应的活性和对映选择性问题仍然是一个长期未能解决的难题。我们认为解决这个反应的关键还是在于配体。而一个恰当的配体不仅能够提供很高的立体选择性,又能提高反应速率。课题组发展的WingPhos能很高效地解决这个问题。在该配体的铑催化剂作用下,一系列手性二芳基或杂环芳基叔醇均以高产率和高立体选择性地得到。课题组利用该方法学首次发展了一个高效、高立体选择性地合成艾司西酞普兰的全新路线。该工作近期发表在《德国应用化学》。
Huang, L.; Zhu, J.; Jiao, G.; Wang, Z.; Yu, X.; Deng, W.-P.;* Tang, W.* Highly Enantioselective Rhodium-Catalyzed Addition of Arylboroxines to Simple Aryl Ketones: Efficient Synthesis of Escitalopram.
Angew. Chem., Int. Ed. 2016, 55, 4527–4531. [doi]
 |
7. 手性α-氨基三级硼酸酯不仅可以作为药物化学中重要的药效基团,而且是很有用的手性中间体。利用不对称催化合成这类化合物的方法仍未报道。α-芳基烯酰胺的不对称硼氢化研究中,我们采用BI-DIME为手性配体 ,首次高立体选择性、高区域选择性地制备了一系列手性α-氨基三级硼酸酯,为药物化学和合成化学提供了重要的手性片段 。此项工作近期发表在美国化学会志上。
Hu, N(1st co-author).; Zhao, G(1st co-author).; Zhang, Y.; Liu, X.; Li, G.; Tang, W.* Synthesis of Chiral α-Amino Tertiary Boronic Esters by Enantioselective Hydroboration of α-Arylenamides.
J. Am. Chem. Soc. 2015, 137, 6746-6749. [doi] |

|
6. 发展新型、高效的反应方法学实现对具有重要生理活性天然产物和药物的绿色合成是我们小组的重要研究目标。在发展新型的不对称交叉偶联反应方法学方面,我们小组设计和发展了一个分子内两芳基间的不对称去芳构偶联,实现了对含有手性季碳中心的菲酮类三环结构的高效不对称构筑,并为萜类天然产物和甾体类药物分子高效合成提供了新的思路。该方法学成功地运用于贝壳杉烯的手性中间体、同化激素宝丹酮和二萜天然产物陶塔二酚的全合成。此项工作近期将发表于《德国应用化学》。
Du, K.; Guo, P.; Chen, Y.; Cao, Z.; Tang, W*. Enantioselective Palladium-Catalyzed Dearomative Cyclization for Efficient Synthesis of Terpenes and Steroids.
Angew. Chem., Int. Ed. 2015, 54, 3033-3037. (hot paper,highlighted by Synfacts ). [doi] |
|
| 5. 在大位阻交叉偶联方面,本组着力发展大位阻芳基烷基间交叉偶联。针对烷基中β氢存在易发生β氢消除这个科学难题,创新性地发展了P,P=O配体,实现了对大位阻芳基和非环状仲烷基之间的交叉偶联,并有效抑制了还原和异构化问题。该方法可以应用于棉酚的新型合成中。此项工作近期将发表于《德国应用化学》。 |
|
Li, C.; Chen, T.; Li, B.; Xiao, G.; Tang, W*. Efficient Syntheses of Sterically Hindered Acyclic Secondary Alkyl Arenes by Suzuki-Miyaura Cross-Couplings.
Angew. Chem., Int. Ed. 2015, 54, 3792-3796. [doi] |
4. 联苯环辛二烯类木脂素具有丰富的生理活性,是一类重要的天然产物,在我国中草药中广泛存在,如五味子素。我们对该骨架的高效构筑感兴趣,因此首次发展了一个高效的镍催化炔铜还原环化的反应。利用本小组发展的手性配体,我们高效地合成了一系列含手性叔醇的呋喃类化合物,并实现了联苯环辛二烯骨架的高效构筑。此项工作近期将发表于《德国应用化学》。
|
Fu, W.; Nie, M.; Wang, A.; Tang, W*. Highly Enantioselective Nickel-Catalyzed Intramolecular Reductive Cyclization of Alkynones.
Angew. Chem., Int. Ed. 2015, 54, 2520-2524. (highlighted by Synfacts).
[doi]
|
3. 本组利用底物间极性-π次级作用,发展了更实用、官能团兼容性更强、高立体选择性的不对称Suzuki-Miyaura偶联催化体系。结合课题组发展的不对称氢化技术,首次成功地应用于手性联芳基类天然产物科鲁普钩枝藤碱A和B、以及马歇尔碱B的高效合成。该方法极有希望应用于一系列手性联芳基类天然产物的简便合成。此项工作近期以封面文章发表在美国化学会志上。
Xu, G.; Fu, W.; Liu, G.; Senanayake, C. H.; Tang, W*. Efficient Syntheses of Korupensamines A, B and Michellamine B by Asymmetric Suzuki-Miyaura Coupling Reactions"
J. Am. Chem. Soc. 2014, 136, 570–573(highlighted as JACS Cover Paper, by Synfacts). [doi]
|
2. 手性β-芳基胺结构广泛存在于药物分子和具有重要生理功能的天然产物中。例如,前列腺增生治疗药西洛多辛(Silodosin)和坦索罗辛(Tamsulosin),慢性阻塞性肺炎治疗药福莫特罗(Arformoterol),帕金森症治疗药物罗替戈汀(Rotigotine)和具有抗HIV活性的科鲁普钩枝藤碱A(Korupensamine A)的分子结构均具有这个重要手性片段。因此,寻找和发展高效的手性β-芳基胺结构的合成新方法一直是个研究热点。利用不对称氢化还原合成(E)-β-芳基烯酰胺是一个简单易得的、很有吸引力和实用价值的方法,但现有的催化体系缺乏足够的效率。 本课题组采用设计深手性口袋膦配体的新思路,发展了C2-对称的新型手性双齿膦配体—WingPhos。其铑复合物在 (E)-β-芳基烯酰胺的不对称氢化中表现出高达99%的对映体选择性和10,000转化数的催化效率。不仅如此,该催化剂在不对称氢化环状以及杂环状β-芳基烯酰胺中表现出很高的效率。该方法可以用来高效合成一系列重要的手性β-芳基胺药物中间体和天然产物的手性片段。此项工作近期将发表于《德国应用化学》。
Liu, G.; Liu, X.; Cai, Z.; Jiao, G.; Xu, G.; Tang, W*. Design of Phosphorus Ligands with Deep Chiral Pockets: Practical Synthesis fo Chiral β-Arylamines by Asymmetric Hydrogenation.
Angew. Chem., Int. Ed. 2013, 52, 4235-4238 (Highlighted in Chin. J. Org. Chem.; Chemistry Portal Highlights). [doi]
|
1. BI-DIME作为一个单膦配体结构特点新颖,活性高,在钯催化交叉偶合上表现出广谱的应用性,对位阻很大的底物表现出特效性。此项工作发表于《德国应用化学》, 受到了很大的国际关注。该论文在2010年11月被国际引文杂志 SYNFACTS选为 SYNFACT of the month,迄今为止被引用次数达66次。
Tang, W.*; Wei, X.; Li, W.; et.al. A General and Special Catalyst for Suzuki-Miyaura Coupling Processes.
Angew. Chem., Int. Ed. 2010, 49, 5879-5883. (Highlighted as;Synfact of the month; by Synfacts in Nov. 2010). [doi]
|
|